高原反应(highaltitudereaction),大家都应该听说过,是人体急速进入海拔3000米以上高原暴露于低压低氧环境后产生的各种不适,是高原地区独有的常见病。轻微症状表现为头痛、头昏、恶心呕吐、心慌气短、胸闷胸痛,严重时会引发呼吸困难,肺水肿,脑水肿等。不同人高原反应也不同。今天给大家介绍的文献就是由一个有趣的人体试验展开的。

鞘氨醇-1-磷酸加快血细胞糖酵解和氧气释放以应对高海拔缺氧环境
Sphingosine-1-phosphatepromoteserythrocyteglycolysisandoxygenreleaseforadaptationtohigh-altitudehypoxia
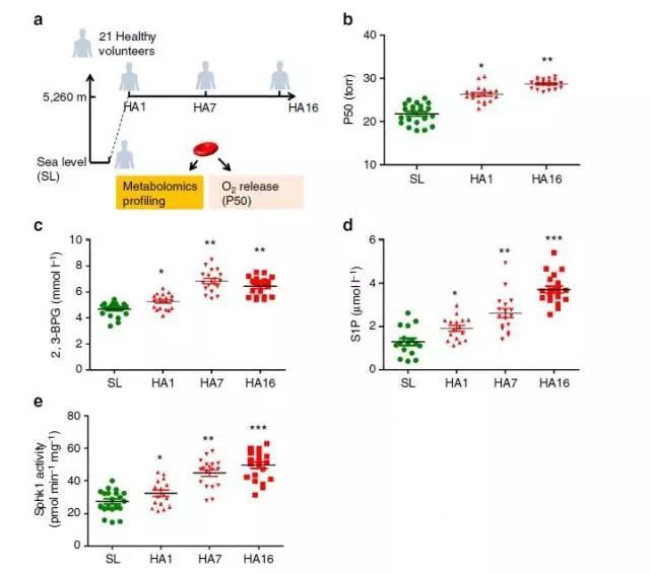
文章作者组织了一批志愿者:21个生活在低海拔地区的健康年轻人,直接转移到高海拔地区(海拔5260m)生活16天;分别在12小时,7天和16天进行红细胞代谢组学和氧释放能力检测。
话说这种免费青藏高原一月游,我也好想去啊~

当志愿者到达高海拔地区后,开始进行检测。结果显示,在12小时内,血细胞的氧释放能力增加了约20%,并在之后的16天中继续增强。非靶向代谢组学检测发现红细胞中2,3-BPG(2,3-bisphosphoglycerate,二磷酸甘油酸)含量在12小时内明显增加,此后一直保持较高的含量。
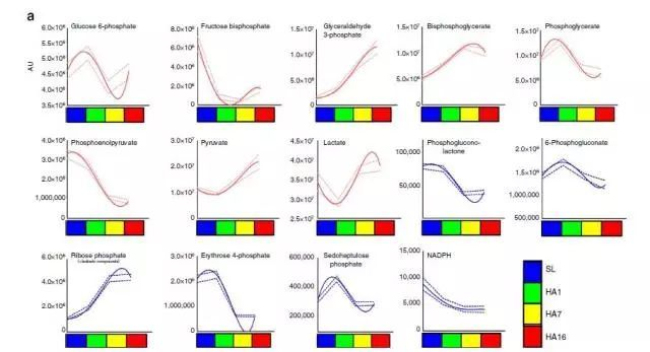
2,3-bisphosphoglycerate可以促进血红蛋白释放氧气,所以这种增加完全正常,此外糖酵解途径代谢物G3P(也是2,3-BPG的上游中间物)显著增加,G3P的上游代谢物glucose-6-phosphateandfructose1,6-bisphosphate以及2,3-BPG的下游代谢物2/3-phosphoglycerateandphosphoenolpyruvate却显著降低;磷酸戊糖途径的代谢物phosphogluconolactone,6-phosphogluconate,erythrose4-phosphateandsedoheptulosephosphate以及NADPH含量也增加,暗示着低氧胁迫会激活糖酵解途径,抑制磷酸戊糖途径,从而增强2,3-BPG的产生。
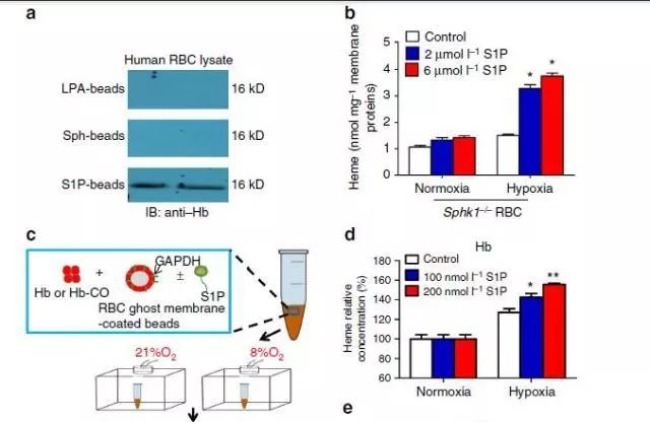
同时另一种物质的增长引起了课题组的兴趣:SIP(Sphingosine-1-phosphate,鞘氨醇-1-磷酸);酶活性检测发现红细胞SIP的催化酶Sphk1(鞘氨醇激酶1)酶活性也有明显的上调。
为了发掘上述人体实验结果所隐含的分子机理,作者在小鼠体内进行了一系列的深入研究:构建Sphk1突变小鼠,低氧实验发现,野生型小鼠与人体实验一致,氧释放增强,SIP,2,3-BPG含量增加,且Sphk1活性增强;突变小鼠却没有这些变化。并通过小鼠间的骨髓移植实验,证实脊髓来源红细胞中的Sphk1调控了低氧胁迫的氧释放。
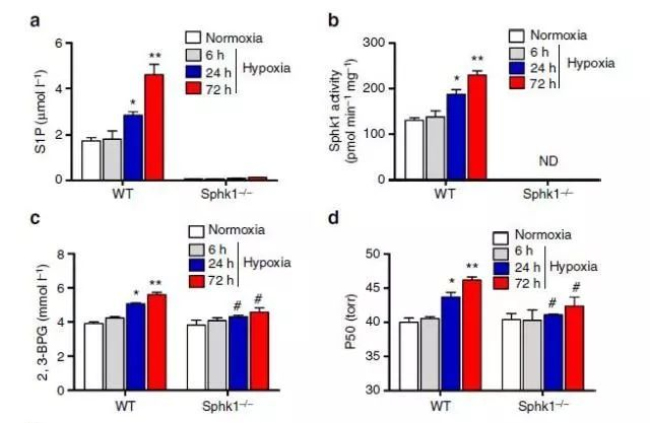
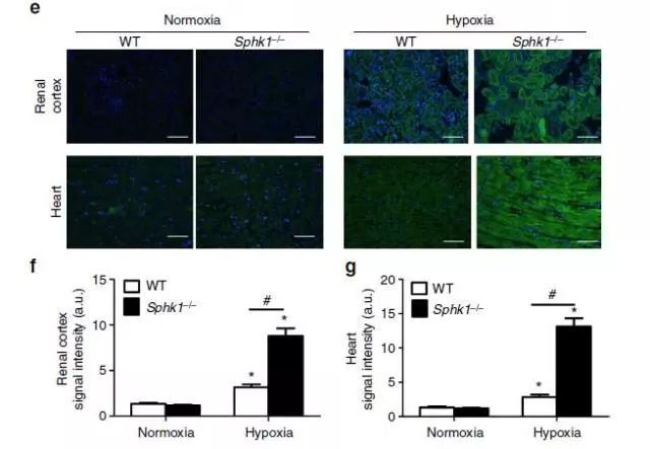
小鼠实验结果
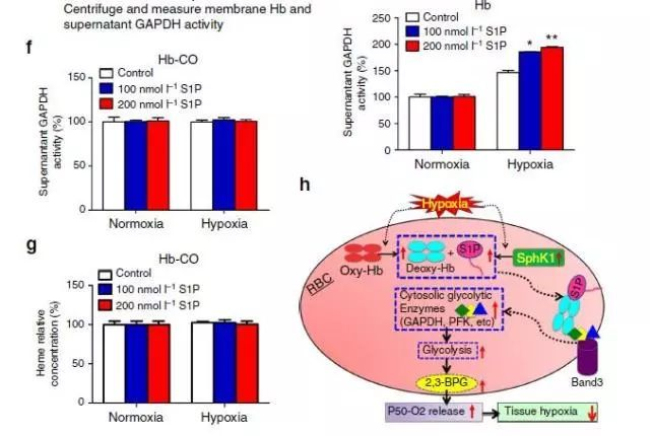
代谢流的实验证明低氧诱导时红细胞中的Sphk1可以使葡萄糖流向糖酵解途径。通过对糖酵解途径关键酶甘油磷酸脱氢酶(glyceraldehyde-3-phosphatedehydrogenase,GAPDH)定位与活性检测试验,以及SIP与GAPDH互作研究,最终解析了一个完整的调控过程:血细胞内SIP会促进去氧血红蛋白附着与膜上,同时释放膜结合的糖酵解酶,增强糖酵解过程生成2,3-BPG,进而促进红细胞的氧释放。
小编心得
本篇文章是非常经典的代谢组机理机制研究范例,前期通过非靶向代谢组学数据,寻找可能的信号/代谢途径,后期通过对目标蛋白的功能分析,解析隐含的分子机理。代谢组学作为与生物表型最接近的组学数据,越来越多机理机制研究以其为起始点,对代谢组学数据的深度分析就是本研究成功打通的关键,非常值得各位老师借鉴学习。





 浙公网安备33010802007965号
浙公网安备33010802007965号