生物标志物(Biomarker)是指“一种可客观检测和评价的特性,可作为正常生物学过程、病理过程或治疗干预药理学反应的指示因子”,作为个体化医疗的“关键词”之一,寻找和发现有价值的生物标志物已经成为当前医学领域的研究热点。
Biomarker的研究现状和发展趋势:
第一个肿瘤标志物可追溯到1846年由HBence-Jones所证实的本周氏蛋白(BenceJonesProtein),对多发性骨髓瘤有一定的诊断作用。170余年后的今天,随着基因组学、蛋白质组学、肽组学、代谢组学等在内的组学平台,以及包括纳米技术、生物信息学、抗体芯片等前沿在内的手段与方法,都为快速获得及筛选生物标志物带来了极大的可能。
基因组学及转录组学描述的是机体可能发生改变的生理指标,而代谢物则是存在于信号通路的终端产物,反映的是机体当时的生理状态。与其他组学相比,代谢组学由于与表型更为接近,因此更适于疾病分型和标志物发现的研究。
2009年,美国密歇根大学霍华休斯医学院研究者基于GC-MS代谢组学研究平台找到前列腺癌biomarker-肌氨酸,发现它癌细胞转移中可能扮演了重要的角色(Nature)。2011年,科学家利用LC-MS代谢组学研究平台找到心血管疾病的预测biomarker,一些磷脂代谢物,如胆碱、氧化三甲胺和甜菜碱(Nature)。2014年,国内研究团队利用GC-MS代谢组学研究平台找到急性髓细胞白血病的诊断biomarker,并通过进一步研究发现肿瘤细胞的另一套代谢机制,揭示出可能的治疗靶点(Blood)。2014年,美国研究团队利用LC-MS代谢组学研究平台,找到4个biomarker可区分肺癌的不同发展阶段,并进行了一千多例的人群验证(CancerResearch)。2016年,国内首批大样本代谢组学研究利用LC-MS代谢组学研究平台,筛选出12组灵敏度高、专属性强的biomarker,可用于临床冠心病的快速诊断以及不同分型的区分诊断(JournaloftheAmericanCollegeofCardiology)。2017年,一个被称为“代谢组学”的代谢动态图像已被用来识别能区分胰腺癌和慢性胰腺炎的新的血液代谢物生物标志物,与传统诊断方法相比具有较高的灵敏度且适用于疾病更早期阶段。研究者报告说,生物标志物特征区分胰腺癌与慢性胰腺炎,假设累积发病率为1.95%,曲线下面积为0.96,敏感性为89.9%,特异性为91.3%。这成功地验证了生物标志物的特征(Gut)。
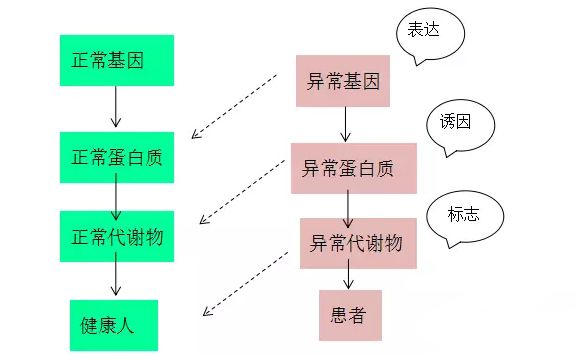
图1遗传疾病中基因型与表型之间的关系
如上图所示,异常的基因不一定产生功能异常的蛋白质;类似的,异常蛋白质不一定会对代谢物造成不利的影响。诱因和这些异常的蛋白质或代谢物的相关程度决定了由诱因预测疾病发生的准确性。
对代谢组进行全面的测定,不仅仅可以用于疾病的诊断,而且可以对疾病从发病到疾病加重过程进行整个过程的监测,分辨出疾病严重的程度,进行及时的预防和治疗。
代谢组学发现Biomarker的研究路线:
代谢组学通过机体代谢物的高通量检测,结合多元统计学分析,筛选差异显著的代谢标志物,进而从整体上深度透析疾病的病理学机理,为疾病的预防及治疗提供了科学依据。研究路线如下图所示:
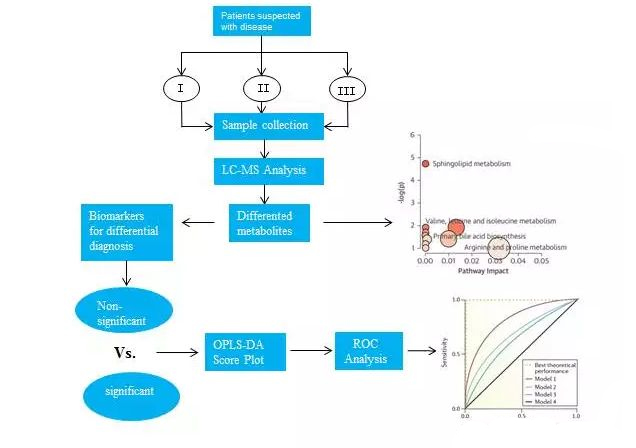
图2代谢组学发现biomarker研究路线
代谢组学在疾病分型和Biomarker发现中的应用:
生命的代谢是一个永不停息的过程。任何疾病的发生和发展都会影响人体代谢,从而导致体液中代谢物质发生显著变化。通过比较机体生理与疾病状态,同一疾病的不同分型、分期的代谢物差异,将能找到与疾病诊断与分型相关的一组Biomarker,用于疾病的诊断与分型。
作为心血管疾病的一种,冠心病是严重危害人们生命与健康的常见疾病,虽然目前通用的数字减影血管造影法确诊率高,但创伤大、花费高、副作用多、操作繁琐。临床急需创伤小、低成本及简便易行的冠心病早期诊断技术。代谢组学方法可通过标准制备的血清、血浆、尿等生物样本可实现高通量小分子物质的检测,这些小分子中许多已经被认为是疾病的危险因子。
美国克利夫兰医院和加州大学洛杉矶分校的学者在筛查人血浆中小分子代谢产物时发现,肠道细菌降解卵磷脂后所生成的“副产品”可预测哪些人未来可能发生心脏病。进一步的动物试验显示,肠道微生物在饮食中的脂质转化为三甲胺N-氧化物(TMAO)的过程中起重要作用,而TMAO可促使导致心血管疾病的动脉斑块的形成(Nature,2011)。上述研究表明,肠道共生菌也可导致或加重包括肥胖、免疫异常等在内的疾病状况,而以TMAO为靶点的药物或可预防动脉粥样硬化和心脏病。
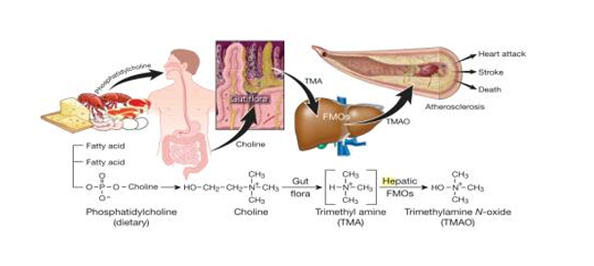
图3膳食PC和动脉粥样硬化的肠道菌群依赖性代谢
那么找到了关键的Biomarker,我们如何更进一步的进行疾病机制的研究呢?在组学的时代,随着基因组学、蛋白质组学、肽组学、代谢组学等在内的组学平台,以及生物信息学的发展,多组学联合分析来解释和阐述疾病病理机制已成为可能。2016年,该团队研究学者在先前的代谢组学研究基础上结合基因组学进行了mGWAS(MetabolomeGenome-WideAssociationStudy)的研究,他们取了3880个冠心病患者的血浆,采用代谢组技术检测胆碱等(8种)代谢物,利用重测序获得材料SNP信息。基于代谢组数据和重测序SNP信息,开展mGWAS研究,最终得出在染色体2q34和5q14.1上发现了两个位点与冠状动脉疾病发展显著相关,甘氨酸代谢与尿素循环可能揭示了新的动脉粥样化硬化疾病发展机制。
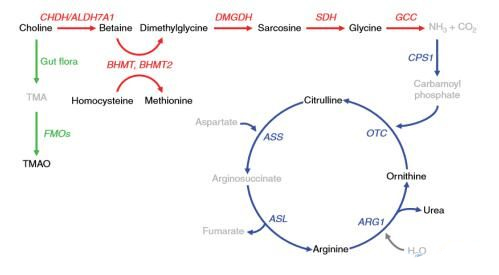
图4连接胆碱代谢途径和尿素循环的基因和中间体
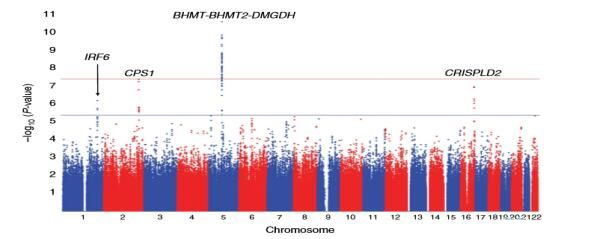
图5血浆中甜菜碱的GWAS结果
除了肿瘤和心血管疾病,近年来随着生活水平的提高,高脂肪、高蛋白质饮食、缺乏运动,以及一些不健康的生活习惯,导致由肥胖、高血压、高血糖等高危因素组成的“代谢综合征”威胁现代人的健康,利用代谢组学的技术手段也可为这些疾病的发病机制、诊断及药物疗效提供新的线索。
“广泛靶向代谢组”技术的优势:
“广泛靶向代谢组”是一种全新的代谢物定性、定量检测技术,它结合了非靶向、靶向的优点,将高通量、高灵敏度和定量的优点集合于一起,特别适合检测中低丰度代谢产物,是发现新代谢Biomarker的最适方法,具有高通量(一次可检测>1000种代谢物)、高灵敏(能检测低丰度代谢物)、广覆盖(可覆盖超过20条代谢通路)、定性定量准(拥有近千种标准品库)等特点。检测的代谢物包括氨基酸及其衍生物、糖、核苷酸及其衍生物、维生素、脂质等物质。
通过基因测序找到疾病的控制基因,通过蛋白测序研究基因如何调节下游的信号通路,最后通过代谢组学分析研究基因表达调控的最终结果。迈维代谢可利用基因组、转录组、蛋白组和代谢组多种组学技术进行联合分析,可对疾病的发生机制有更全面的认识,对疾病的诊断、监测和治疗寻找新的切入点。
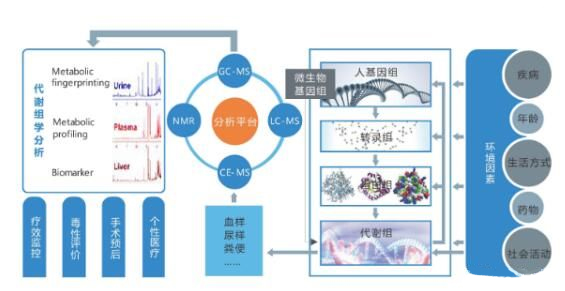
图6代谢组学与多组学结合助力医学研究





 浙公网安备33010802007965号
浙公网安备33010802007965号