Metabolomics as a Driver in Advancing Precision Medicine in Sepsis
期刊:Pharmacotherapy
研究背景
脓毒症是世界上主要的死亡原因之一。脓毒症患者通常需要在重症监护病房(ICU)接受治疗。脓毒症所需要的重症监护医疗总费用很多,接近美国国内生产总值的1%。此外,脓毒症的发生率与人口老龄化和人口数量增加是一致的。最易感染败血症的人群包括老年人和新生儿。美国儿童脓毒症的诊断率为0.56‰,死亡率为10.3%。在成人中,脓毒症的发生率为18.6‰,在暴发性感染性休克中死亡率高达50%。
脓毒症的病因和定义
脓毒症的病因因年龄而异,可包括细菌、病毒和真菌病原体。在儿童最常见的病原菌是葡萄球菌种,其次是真菌感染,后者在患癌症的儿童中更为常见。病毒病原体在年轻人中很常见,但儿童常伴有细菌共感染。在成人中,大约有一半感染由革兰氏阳性细菌引起,约40%由革兰氏阴性细菌引起,超过6%来自厌氧菌和真菌。虽然引起脓毒症的病原体没有明显变化,但脓毒症的定义经过20多年发研究才更新。由于该领域新知识的出现对其定义进行重新评估。然而,这些修订后的第三国际共识(脓毒症-3)定义仅适用于成人。此外,分类严重脓毒症在最近的成人定义中有所减少,但在儿科定义中仍然存在。
由于脓毒症的内在异质性和缺乏诊断的黄金标准,儿童和成人脓毒症的诊断、风险分层和治疗都具有挑战性。传统上,这导致了较差的临床结果,并导致了大量药物治疗失败的临床试验。诊断和预后工具很少,主要基于临床体征和症状。根据年龄的不同,这些参数在儿童中可能有所不同。例如,8个月大婴儿的心动过速定义为每分钟>180次,而3岁婴儿的心动过速定义为每分钟>140次。此外,尽管序贯器官衰竭评估(SOFA)评分对重症监护病房治疗的成人患者的预后具有预测作用,但对脓毒症患儿的预后还不够。儿童器官功能障碍评分是目前唯一在临床试验中得到验证的儿童评分系统。总的来说,评分系统的使用很麻烦,通常不作为病人护理的一部分。因此,Sepsis-3专责小组建议,SOFA得分≥2作为脓毒症标准,因为它可以从临床数据计算更容易获得。然而,这些临床工具的准确性较低,这给脓毒症的精准治疗带来了特殊的挑战,也阻碍了针对特定亚群人群的药物治疗的识别。例如,脓毒症患者的免疫反应从过度活跃的炎症级联反应到高度免疫抑制的表型。这些表型最初可能不容易在床边鉴别或与可观察到的临床参数相关。脓毒症的早期准确诊断可影响临床决策,指导更准确的治疗干预。因此,更准确的表型脓毒症的新方法有巨大的需求。包括代谢组学和药物代谢组学在内的系统生物学和药理学科学在帮助确定特定脓毒症表型方面具有巨大的潜力,并发现非常重要的可预测和预后的生物标志物,这些标志物可导致更个性化的管理和治疗。在本文中,我们将概述目前对脓毒症的认识,以及代谢组学和药物代谢组学在推进脓毒症精准治疗方面的作用。此外,我们还在随附的病例报告中描述代谢组学在小儿脓毒症及时诊断中的应用。
代谢组学介绍
代谢组学是一门系统生物学的科学,它测量和研究单个生物样本中的内源性小分子。代谢组是指任何给定的生物液体、细胞、组织或有机体中的一整套代谢产物。这些小分子,或代谢物,通常小于1000道尔顿,是由代谢过程(如三羧酸循环)和复杂的生物相互作用以及宿主和微生物之间的相互作用产生的。在基因组学中,基因突变可能对蛋白质或蛋白质组学的功能影响很小或没有影响,而蛋白质组学可能无法识别蛋白质的功能变化,临床代谢组学则不同,它检测对内部和外部因素的生化反应的直接结果。此外,几乎任何类型的生物样本都可以被检测,包括血液、尿液和组织。
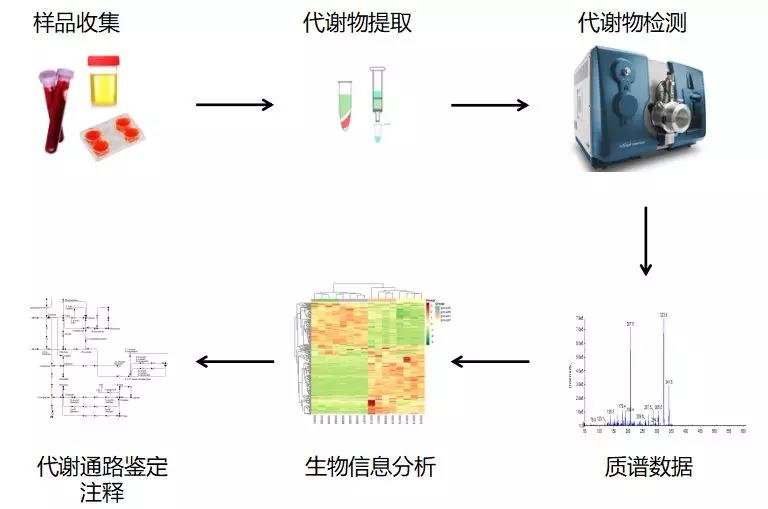
代谢组学研究步骤从样本收集开始。标准操作程序是至关重要的,多中心研究尤其重要, 其迅速、一致的样品处理和存储条件(-80冰箱)尤为重要。对于特定的分析平台,除尿液外,大多数情况下,在分析前需要从样品中去除大分子。有许多选择,包括样品超滤或甲醇沉淀。选择取决于样本的类型(例如,组织样本需要更多的处理)和代谢组学研究的目标。例如,如果血清样本被过滤,脂质代谢产物将被保留并丧失在过滤器中,而使用甲醇-氯仿萃取将产生样本的水和非水部分,这就允许从单一样品中对水样和脂质代谢产物进行双平台分析。代谢物可以通过多种不同的分析平台进行测量,其中最常见的两种是一维(1D)质子(1H)核磁共振(NMR)光谱和质谱(MS)。尤其适用于分子量小于100道尔顿的中高含量代谢物、极性化合物的检测,而液相色谱质谱联用(LC-MS)可能会漏掉这些代谢物。然而,尽管每个化合物都具有独特的NMR谱,识别和量化复杂混合物中具有重叠谱峰的代谢物也具有挑战性。
使用商用光谱处理和分析软件,如Chenomx(www.chenomx.com)核磁共振套件8.0(加拿大艾伯塔省埃德蒙顿Chenomx公司)可用于从原始核磁共振光谱中优化代谢产物的识别和定量。质谱平台,如气相色谱质谱联用GC-MS和液相色谱质谱联用LC-MS比核磁共振更敏感,因此更适合测量观察代谢物的检测(< 5μM)如脂质和挥发性化合物。目前,LC-MS通常用于所谓的“非靶向”代谢组学,因为它可以有效地检测多种不同类型的代谢物。分析和光谱处理技术正在迅速发展,可以同时检测水和脂类化合物。此外,目前还没有通用的LC-MS代谢物文库可以应用于不同的仪器。这使得代谢产物鉴定和定量尤为重要。更多的细节,读者可以参考分析代谢组学的最新评论。1H-NMR光谱采集相对简单,但需要遵循一些规范(如脉冲序列)。这对于定量的核磁共振代谢组学是至关重要的,而定量的核磁共振代谢组学需要一个可靠的内部标准峰。如果在各个临床中心做的都是正确的,那么这些数据是高度可复制的。LC-MS的光谱分析比NMR更加自动化。大多数LC-MS仪器制造商都有专门的软件来查找和命名峰值。然后使用已知的标准确认代谢物的识别和定量。
代谢组学数据集生成后,下一步是统计分析,这可能非常复杂,通常从主成分分析(PCA)和偏最小二乘判别分析(PLS-DA)等非监督和监督学习方法开始。无监督方法有助于基于数据驱动的组分类和数据中存在的趋势来描述数据。除PCA外,其他常见的无监督方法有k均值聚类和层次聚类。使用监督学习方法来确定已识别代谢产物的预测能力和结果(例如,脓毒症vs不脓毒症,或严重脓毒症vs脓毒症)。这些方法包括(O)PLS-DA和支持向量机,通常用于发现候选的生物标志物。
这些分析通常使用定性代谢组学数据进行,称为化学计量分析。然而,可以使用非参数和参数统计代谢组学数据分析,特别是对定量数据的分析,以识别不同的代谢产物。在此之前进行数据转换(例如,日志规范化和范围缩放)以实现正态分布。在生成p值之后,需要采用一种方案进行多次比较的校正,例如计算错误发现率。代谢组学数据分析可以使用包括MetaboAnalyst (http://www.metaboanalyst.ca/)在内的许多公开可用的平台来完成。这种严格程度对于测试可重复性和构建生物标志物凭据所需的预测模型的测试是至关重要的。统计分析后,使用Metscape (http://metscape.ncibi.org/)等工具进行路径映射,可以使用Cytoscape (http://cytoscape.org/)插件可视化代谢组学数据及其相关代谢通路。
虽然上述方法的总体原则是不变的,独立于正在研究的疾病过程,但在研究脓毒症的代谢组学时,有一些具体的考虑。患者在医院内的位置和采集样本的时间是需要考虑的重要因素。与其他一些使用代谢组学(糖尿病、心血管疾病)研究的疾病状态不同,在脓毒症的研究中,采样时间是关键,因为疾病的快速进展会影响关键的代谢途径。此外,刚到急诊科的新发现的脓毒症患者可能与在重症监护室接受几天多次干预治疗的患者有明显不同的代谢组学特征。
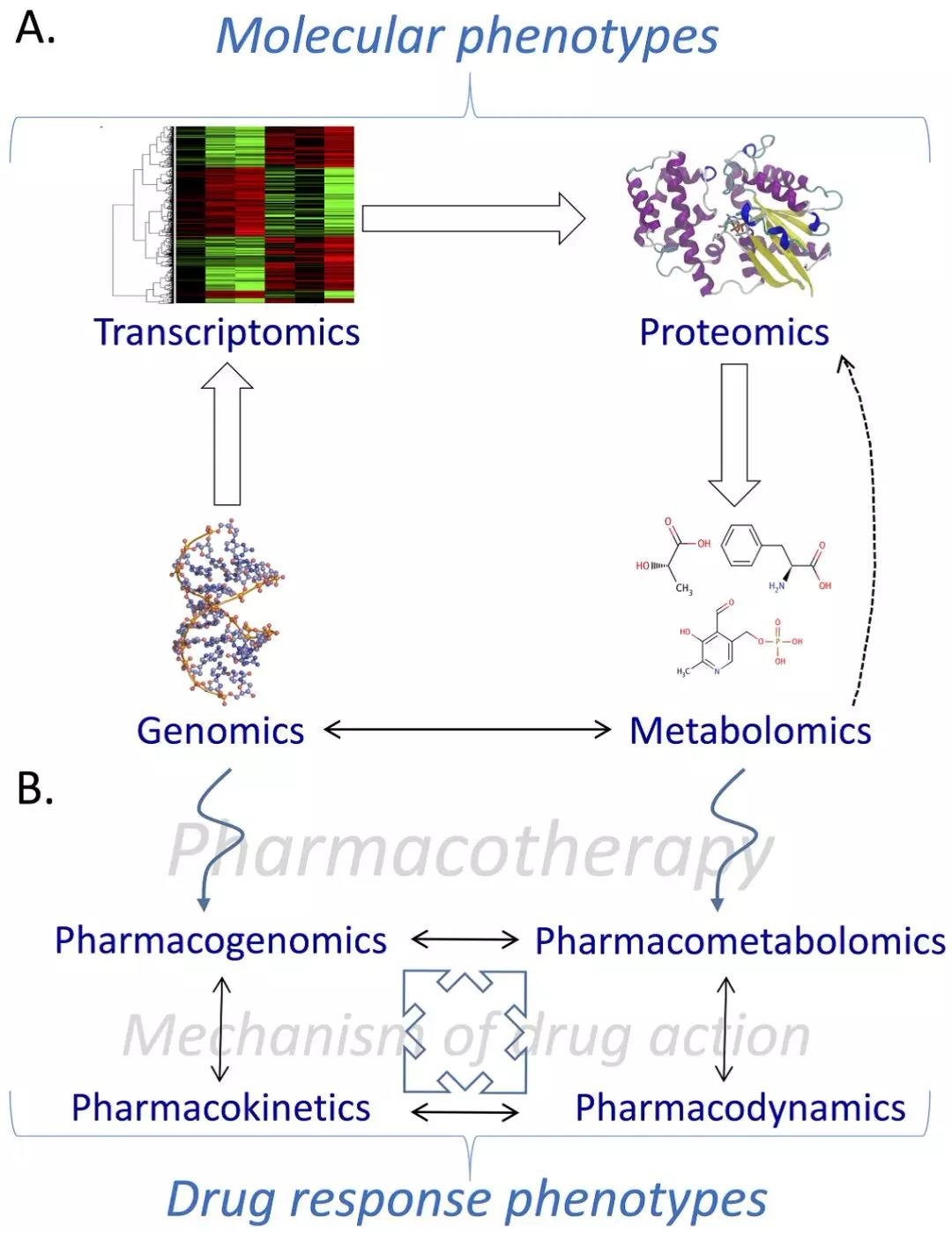
药物代谢组学是代谢组学在药物反应预测中的应用。以上所述的代谢组学在研究设计、工作流程和分析方面的原则都适用于药物代谢组学。尽管药物代谢组学的严格定义将其限制在预测范围内,但需要注意的是,为了准确可靠地预测药物反应,需要对药物代谢变化和表型差异与预处理代谢物水平之间发现的关联程度进行前瞻性检验。除了药物反应的预测,药物代谢组学可能是一个特别强大的工具,无论是单独或与其他系统药理学科学相对,对于了解各种药物反应、药物作用机制和药物不良反应的机制提供基础性知识。
脓毒症的代谢诊断
炎症反应可由无菌炎症(手术、创伤)或感染(脓毒症)后遗症引起,生命体征异常可作为炎症反应的证据。因此,成人和儿童在临床上都难以识别潜在感染患者,也难以通过脓毒症确定病情进展的可能性。由于缺乏有效的诊断试验和血液中细菌的低检测率,脓毒症的诊断尤其具有挑战性。代谢组学有潜力为指导这一关键的临床决策提供信息。
在人类和动物的研究中,代谢物谱一致地显示了鉴别无菌炎症和脓毒症的能力。在创伤后入住ICU的成年人中,入院时代谢物谱成功地鉴别出哪些人出现了脓毒症,哪些人没有。在儿童中也发现了类似的差异,代谢物谱清楚地区分了脓毒症和无菌炎症以及幸存者和非幸存者。在新生儿中,代谢物谱将健康对照组与脓毒症患者区分开来,并在早发和晚发脓毒症之间显示出不同的模式。在早期脓毒症的成人和儿童中,参与能量代谢的代谢物表现出一致的方向变化。酮体增加,柠檬酸盐、戊糖磷酸途径化合物、利比妥和核糖酸的水平降低。几项研究已经确定了葡萄糖、乳酸、乙酸、柠檬酸和代谢物,区分败血症和全身炎症反应综合征(SIRS),这些发现提出了在小儿脓毒症的情况下,NMR尿液代谢组学检测到能量代谢的变化,包括酮体水平的增加,从理论上讲,它可以辅助早期诊断脓毒症的病人。
代谢组学用于脓毒症的预后监测
最终,临床医生感兴趣的短期结果是死亡率和末端器官损伤。这些结果的出现与特定的病原体无关,可能是由于病原体、患者和环境之间的复杂相互作用。对临床医生来说,尽早识别高危患者是有益的。进展性脓毒症患者的代谢物谱与病原无关,而和不同的代谢物谱可识别脓毒症导致的特定终末器官损伤程度相关。最近,脓毒症的长期有害后果在幸存者中变得明显。具体来说,病人表现出认知和功能受损。当然,脓毒症生存的长期预后和预测生物标志物将具有很大的价值,特别是如果能够确定药物治疗的靶点。这些发现在一定程度上可能在于代谢组学对脓毒症病理生理学的新见解,这反过来可能为靶向治疗提供新的领域。
代谢组学已经确定了健康受试者和脓毒症患者之间,以及脓毒症幸存者和非幸存者之间能量代谢的差异。这些代谢产物主要是氨基酸及其衍生物,在脓毒症的病理生理过程中起着能量代谢的作用。在与健康对照组的成年人进行内毒素血症和社区获得性脓毒症的比较时,确定了特定的代谢产物,代谢产物的变化方向也类似。比较生还者和非生还者,发现游离脂肪酸代谢发生改变,提示非生还者线粒体脂肪酸beta氧化存在严重缺陷,糖酵解、糖异生和柠檬酸循环也有差异。此外,犬尿氨酸,一种色氨酸代谢的副产物,也可区分SIRS(表1)和脓毒症,在非幸存者中高于幸存者。我们也在成人脓毒症休克患者中证明了这一点,在治疗前酮体水平升高的患者中,补充左卡尼汀似乎效果较差,这意味着有证据表明能量代谢中断的患者更不可能在脓毒症中存活。
最后,代谢组学在脓毒症中对儿童和成人的优势和“附加值”可能是当它与临床数据和其他测量相结合时,以改善对结果的预测,并证明与目前可用的诊断测试(包括降钙素原、c反应蛋白和乳酸水平)相比,其表现有所提高。在这一策略的一个例子中,使用代谢组学和炎症蛋白介导物在急诊科就诊后早期对儿童进行分析,区分了需要和不需要ICU护理的儿童。代谢组学的这一应用可能有助于败血症的分类决策和风险分层,尤其是在没有儿科专业知识的临床环境中。
脓毒症的精准医疗和药物靶点
代谢组学的一个更有趣的方面是,它有可能提供有关个人治疗资格和反应的早期临床相关信息。随着目前对耐药病原体和抗生素管理的关注,药物代谢组学可以允许早期定制和靶向治疗,从而降低耐多药生物的流行率。在大多数感染病例中,在开始治疗后数天至数周内无法获得病原体检测诊断试验的结果。重要的是,只有在培养出该微生物并获得其敏感性之后,才能获得指导抗菌治疗选择的具体信息。通常,特别是在儿童中,没有确定具体的病原体或培养是阴性的。在真菌感染的情况下,可能几周内无法得到确切的结果。
在一项对新生儿真菌感染的研究中,与健康对照组相比,丝氨酸的含量升高,而在抗真菌治疗的反应中,丝氨酸的含量逐渐下降,在培养结果最终确定之前,它提供了针对治疗的反馈。在动物研究中,接受有效和无效抗生素治疗的小鼠在治疗开始后2小时内对金黄色葡萄球菌表达代谢物表现出差异。同样的,作者能够证明在体内治疗对金黄色葡萄球菌和大肠杆菌感染的反应有类似的变化。随着脓毒症新疗法的开发,代谢组学可以作为一种工具,阐明影响的生化途径,监测不良事件,预测和跟踪治疗反应性,并促进脓毒症的精确药物方法。
此外,药物代谢组学与其他系统药理学科学的结合,如药物动力学和药物基因组学,可以进一步细化药物反应表型。由于确定可行的药物靶点是药物发现的关键,代谢组学在这方面可能特别有用。例如,在一项动物研究中,发现红细胞生成素可以减少败血症中末端器官的损伤,并且在治疗组和未治疗组之间发现了明显的代谢谱改变。此外,在鉴定代谢物的基础上,鉴定了促红细胞生成素影响的具体途径。这一发现可能会导致对实验疗法的进一步研究,也为其他疗法的发展提供新的假设生成数据。在一项补充肉碱治疗成人感染性休克的I期试验中,治疗前代谢物谱在对治疗有反应和无反应的患者之间存在差异。
区分肉碱应答者和无应答者的代谢物影响生物化学途径,这些途径可能有助于识别肉碱无应答患者的药物靶向机会。重要的是,在治疗前,有反应者和无反应者之间没有明显的临床差异。这一发现为进一步的研究提供了方向,因为代谢组学可以帮助早期识别最可能对特定疗法有反应的患者,而这些患者在临床上并不容易使用传统方法进行区分。确定对特定治疗有反应者和无反应者的代谢表型,可以再次提供见解了解脓毒症生理学的差异,指导更有针对性的精确治疗,从而提供一种方法来克服被认为是导致临床试验反复阴性的主要障碍,即患者群体的异质性很大。将代谢组学作为纳入标准可减少研究患者的异质性,提高临床试验成功的可能性。
未来方向
作为一种诊断工具,代谢组学已显示出巨大的潜力以区分患者的败血症和无菌炎症(如SIRS),并预测死亡率。以我们的病例报告为例,代谢组学可用于预测成人和儿童脓毒症的病情严重程度以及不同的病原体来指导适当的抗菌治疗,并确定评估治疗反应的最佳时机。与其他系统生物学方法相比,代谢组学最接近于解释个体、环境和病原体之间的直接相互作用。正是这些特点使其在脓毒症的异质性评估中发挥作用。随着这一领域的发展,药物代谢学——代谢组学在药物反应预测和表型方面的应用——可能会成为系统药理学中越来越重要的一员。
代谢组学在成人和儿童患者的临床应用中面临的一个挑战是获得及时和可获得的结果。目前,代谢组学工作流程较长,不利于生成用于临床决策的实时数据。重要的是,随着药物反应、诊断和预后的关键鉴别代谢物的识别,代谢物的识别和定量的确认将是必不可少的。此外,代谢组学研究的发现需要在前瞻性研究中得到验证,以实现可靠的生物标志物认证。新技术正在开发中,包括可编程纳米生物芯片和芯片上的新陈代谢技术。随着代谢组学在未来治疗干预研究中的应用,代谢表型可能成为临床试验中对受试者进行基准或风险分层的有用工具。
原创: 郭锐 迈维医学





 浙公网安备33010802007965号
浙公网安备33010802007965号