卵巢癌为激素相关性肿瘤,是妇科肿瘤中的头号死因,其发病隐匿、发展迅速、预后差,早期无特异表现,出现症状多已属晚期。70%的患者就诊时已是III期或IV期。尽管有了良好的手术治疗和化疗,但这部分患者的五年生存率还是在20%-40%之间,而I期的卵巢癌患者5年生存率可达90%。因此,有效地进行早期诊断对提高卵巢癌患者生存率具有重要现实意义。
目前,在卵巢癌早期诊断方面尚无有效方法。尽管有了很多新技术,但在卵巢癌的筛查中很难找到一种特异性和敏感度都高的单一指标。病理学检查是金标准,虽然影像学技术对卵巢癌的检出有所帮助,但是所需仪器设备及技术条件要求高、费用贵,不适用于普查。肿瘤标志物之一的糖蛋白是一类含糖的蛋白质,目前在卵巢癌诊断中的常用的糖蛋白有CA125、HE4、CA724、CA199等。CA125是目前FDA批准的生物标志物,用于临床监测对治疗和复发的反应,但其对患者生存的影响有限,同时CA125的假阳性率高。所以迫切需要发现HGSC(高分级浆液性卵巢癌)早期诊断生物标志物的新策略。

近日,来自加拿大的Thomas Kislinge教授团队在国际学术期刊Cell Systems(IF=8.982)发表了文章。在该研究中,他们描述了一种蛋白质组学策略,用于检测HGSC患者来源的异种移植模型(PDX)血清中的肿瘤相关蛋白,同时使用来自HGSC患者的两个独立的纵向血清队列,证明了概念验证的适用性。研究成果为高分级浆液性卵巢的早期诊断带来了希望。
Kislinge教授就职于加拿大最大的肿瘤治疗和研究机构玛格丽特公主癌症中心,他的团队主要致力于将蛋白质组学技术应用于癌症和心血管方面的研究。鉴于血清蛋白质组的复杂性,研究者开发了一个蛋白质组学工作流程,即使用临床相关的HGSC PDX模型直接识别肿瘤相关蛋白。使用原位移植的PDX模型,他们可以在小鼠血清背景中轻松识别“人类独特的”蛋白质,从而克服与基于蛋白质组学的生物标记物发现相关的限制。这种策略使他们能够识别潜在的新型肿瘤相关蛋白。最后使用合成的、稳定的同位素标记的肽,他们能够快速开发用于HGSC患者血清中定量的靶向蛋白质组学测定。

一、基于PDX的N-糖蛋白组策略以检测血清中的肿瘤相关蛋白
相关研究表明,细胞膜和细胞外基质的蛋白质通常是N-糖基化的,并且这些蛋白质可以分泌或脱落到细胞外环境中。因此,基于N-糖的富集可以是检查血清中组织渗漏蛋白的有效策略。利用这一原理,作者开发了一种检测肿瘤相关蛋白的新方法。简言之,产生12种不同的PDX模型(手术切除HGSC肿瘤并进而植入小鼠腹膜内),在终点收集肿瘤组织(PDX-肿瘤)和血清(PDX-血清),以来自非移植的同基因小鼠的血清(NEGsera)作阴性对照(样本策略),运用label-free定量蛋白质组加以分析(质谱策略)。
正如预期的那样,与对照组NEG血清相比,PDX-血清样本与PDX-肿瘤样本存在显著差异。各样品类型中共鉴定到3922个去糖基化位点,其中绝大部分去糖基化位点(约2077多个位点)仅在PDX-肿瘤中发现分布。PDX-肿瘤和PDX-血清中定量到649个位点,表明这些肽可用作HGSC生物标记物(图1D)。总之,基于PDX的N-糖蛋白组策略可以检测血清中的肿瘤相关蛋白。
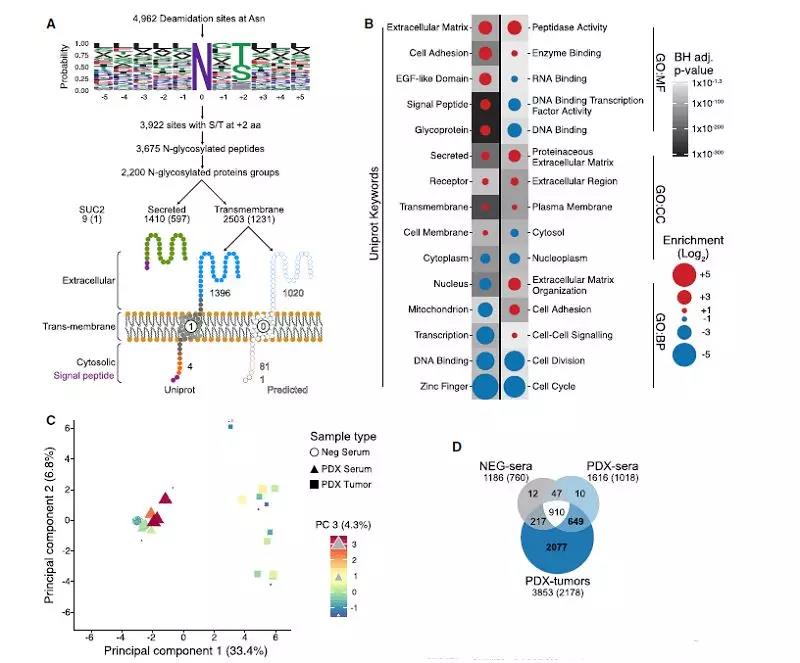
图 1 N -糖肽的蛋白质拓扑定位与N-糖蛋白组的功能分析
二、细化物种分配以及PDX-血清/肿瘤中去糖基化位点的强度分布
由于最初的peptide assignment使用人和小鼠相连的方式,并在UniProt-同种型蛋白-FASTA数据库(66763总序列)中进行,显然这不是非常全面的,所以作者一步改进了物种匹配。该改进包括将检测到的肽序列与更全面的蛋白质序列数据库匹配,通过他们的优化,将39个人类独特的去糖基化位点的物种分配改变为人-小鼠保守,同时也将两个小鼠独特的去糖基化位点改变为人-小鼠保守(图2E)。
与PDX-肿瘤相比,去糖基化位点在PDX-血清中具有更大的动态范围(图2F与图2G,上图对比)。经典小鼠血清蛋白(即C4b,Mug1和Serpina3k)的去糖基化位点偏向PDX-血清中的较高强度,而HGSC相关蛋白(即FOLR1,CA125和MSLN)分布在中等至低-强度点。这些结果表明肿瘤相关蛋白会释放到血液中,但是以较低浓度存在。然而,对PDX-肿瘤中去糖基化位点强度的类似分析显示物种分布更均匀(图2G,底部),表明移植的肿瘤相关蛋白和宿主衍生的基质蛋白的丰度在肿瘤组织中更相似。
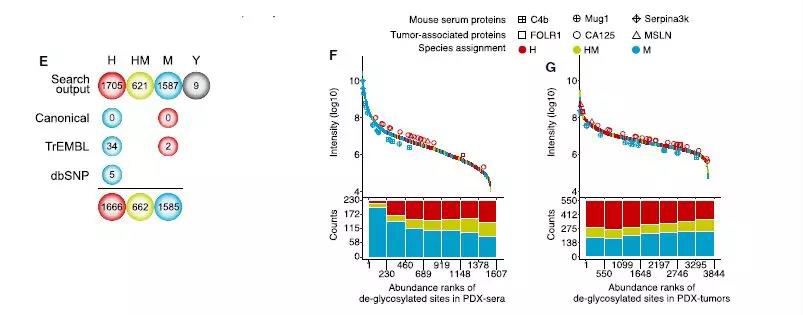
图 2 PDX-血清/肿瘤中去糖基化位点的强度分布
三、从PDX样品中选择肿瘤相关蛋白
通过生物信息学分析,作者获得了PDX-血清中各种丰度的蛋白质功能注释。作者将小鼠蛋白质定位到它们的人类直向同源物中,产生总共745种独特的蛋白质(图3A,左)。Acute-phase(参与炎症的基因)、蛋白酶抑制剂、补体系统和丝氨酸蛋白酶是其中丰度相对较高的蛋白质。与之相反的是,细胞表面、细胞间粘附分子、金属蛋白酶、受体、ECM组分和信号素等组织渗漏和信号传导相关蛋白在其中以中、低丰度存在。
有趣的是,更高丰度的蛋白通常来自于鼠源,验证了他们之前发现的PDX-血清蛋白质中的物种偏倚(图3A,右)。比较PDX-血清和PDX-肿瘤中定量到的1559个去糖基化位点的强度,表明人类独特的去糖基化位点在PDX-肿瘤中具有更高的强度(图3B)。接着,作者想使用获得的蛋白质组学数据从HGSC PDX模型中选择候选肽用于开发靶向蛋白质组学测定(图3C)。总之,通过对HGSC PDX模型的比较和功能分析,他们鉴定了一组肿瘤相关肽,用于系统开发靶向蛋白质组学测定。
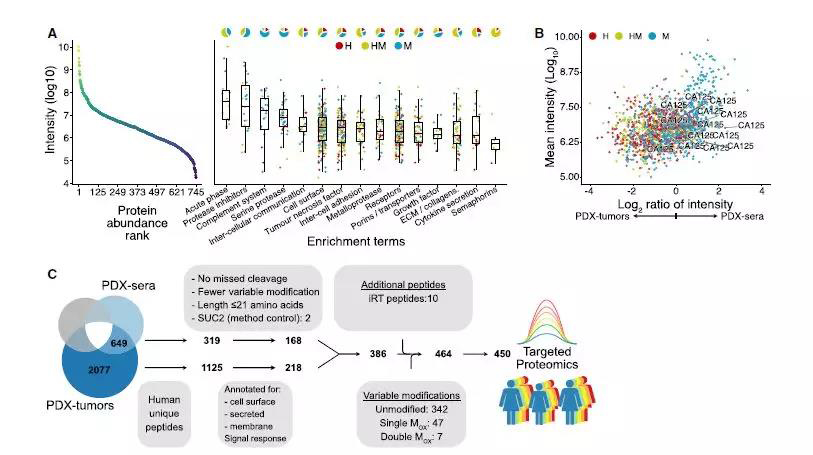
图3 潜在标志物的选择
四、PRM靶向蛋白质组学分析
为了能够对来自HGSC患者的血清中的肿瘤相关肽进行定量,作者使用平行反应监测质谱(PRM-MS)系统地开发了靶向蛋白质组学测定(图4D)。他们通过优化色谱梯度和标准化碰撞能量(NCE)来最大化测定响应,并通过使用稳定同位素标准(SIS)肽评估测定特异性。研究者快速开发了通过基于PDX的N-糖蛋白组学策略发现的408种肽的PRM-MS分析,成功率为90%(408/450)(图4H)。
最后,在一项小概念验证研究中,他们将这些靶向分析应用于来自HGSC患者的两个纵向血清群组(n = 20,96血清)。他们证明通过基于PDX的N-糖蛋白组学策略发现的候选肽可在人血清中定量,并且通常也能模拟当前HGSC生物标志物CA125的表达谱。
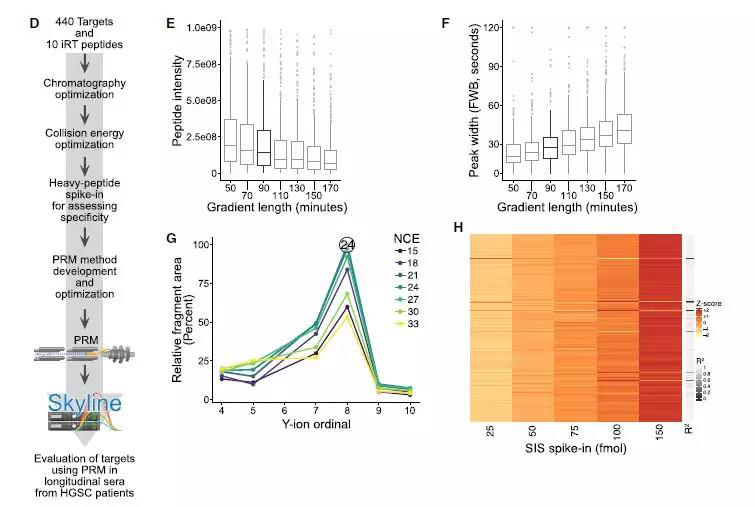
图4 靶向蛋白质组学分析
总而言之,本文通过对HGSC PDX模型的比较和功能分析,使其能够识别潜在的新型肿瘤相关蛋白,配合使用合成的、稳定的同位素标记的肽,用于系统开发靶向蛋白组学检测。当然这一策略仍旧需要在更大的患者队列中进行验证。
同时有理由相信,他们的实验策略应该也能适用于具有可用PDX模型的其他癌症类型。但不得不指出的是,这种策略也具有一定潜在的缺点(基于PDX的肿瘤相关蛋白的鉴定,通常上限于分析源自移植人癌细胞的人类独特候选物)。总之,他们提出的这一方法,可以为开发新的HGSC早期筛查标志物带来可能。
参考文献
1. Zhang, H., et al. (2016). Integrated proteogenomic characterization of human high-grade serous ovarian cancer. Cell.
2. Sinha A, et al. (2019). N-Glycoproteomics of Patient-Derived Xenografts: A Strategy to Discover Tumor-Associated Proteins in High-Grade Serous Ovarian Cancer.Cell Systems.
原创: Dr.Proteomics 精准医学与蛋白组学





 浙公网安备33010802007965号
浙公网安备33010802007965号