蛋白质组学是中心法则的中间位置,也是精准医学研究的核心内容,为癌症早期发现、良恶性诊断、分型和个性化用药、疗效监测和预后判断等提供了更精确、更可靠的信息,使精准医学更加精准。
蛋白质组学在医学研究最常见的两种模式:
一是通过蛋白质组学、修饰组学寻找疾病发生发展的新型标志物,这种研究思路就是通过收集血液、尿液等各种体液,通过4D-LFQ、Label-Free、TMT等高通量蛋白质组学技术对体液中的样本进行鉴定和定量,并结合PRM靶向蛋白质组学对潜在标志物进行验证,目的是找到新型的用于疾病诊断、发展、分型、治疗指症以及预后的标志物。研究的思路清晰,问题在于大样本的收集,分组以及临床信息的采集和分析。
二是建立疾病或者研究主题的表达谱、分子机制和潜在靶点。这种研究思路在于通过检测病理样本与正常样本间的蛋白表达差异或动态变化过程,寻找疾病相关的关键因子,再结合进一步的机制研究,揭示关键因子的调控机制,全面的了解疾病的发生发展过程。
今天我们结合两篇最新的高水平文章,来简单介绍一下。
1、Science Advances: 蛋白质组学揭示癌症的性别差异之谜
众所周知,疾病存在性别差异。美国国家癌症患者数据库的分析数据显示,男性比女性更容易患上癌症,而且男性对癌症的预后结果也比女性要差。然而导致这种差异的机制尚不清楚。
8月14日,国际专业学术期刊Science Advances上的一项研究,就从分子层面找出了一种潜在的机制。西班牙巴塞罗那生物医学研究所的研究人员,运用蛋白质组学等方法,鉴定出导致两性肿瘤恶化程度不同的调节因子Phf7,可能是减轻肿瘤恶性程度的潜在靶点。

研究者利用模式生物黑腹果蝇(Drosophila melanogaster),以脑瘤为例考察了癌症恶化的性别差异,通过在果蝇的脑中诱发出肿瘤,然后比较雌雄两性中肿瘤的发展过程,结果表明雄性果蝇脑中的肿瘤具有更强的侵袭性。研究人员进一步运用TMT标记的定量蛋白质组学方法,比较野生型与不同性别的肿瘤细胞中的蛋白质表达水平,找出在雌性和雄性中明显有差异的蛋白质。
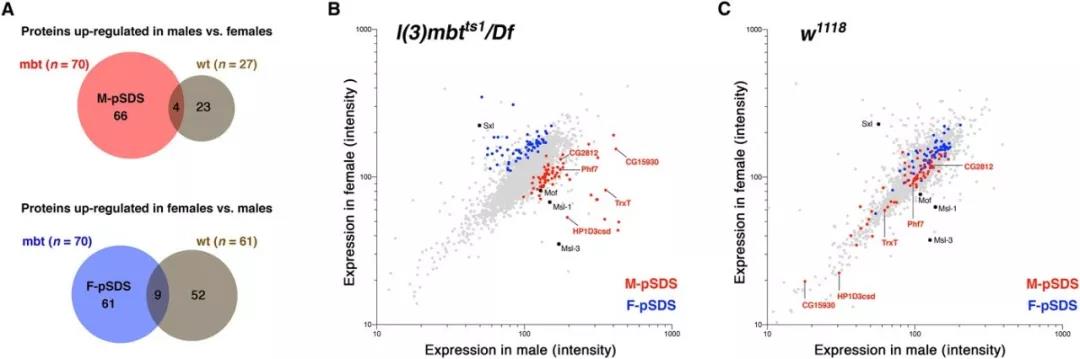
雄性果蝇(红色)和雌性果蝇(蓝色)的致死性恶性脑瘤的蛋白质组学分析
研究共鉴定到7035种蛋白质,并获得了5985种蛋白质的可靠定量数据。127种蛋白质在雄性和雌性中表达水平显著不同,其中66种蛋白质在雄性中表达较多,61种在雌性中过度表达。研究人员发现,Phf7蛋白(PHD finger protein 7)在雄性果蝇的肿瘤细胞中表达明显高于雌性。当把雄性果蝇体内的这种蛋白质去除后,原先侵袭性强、容易恶化的肿瘤特征得到了有效抑制。雄性果蝇的致死率从93%锐减到38%,与雌性果蝇接近。
值得注意的是,尽管这些潜在的调节因子是在果蝇模型中发现的,很多蛋白质在进化上高度保守,同源蛋白同样存在于人类体内。如Phf7蛋白存在于男性的生殖细胞中,与侵袭性较高的男性肿瘤有关。因此,研究有助于通过调节癌症性别差异的关键蛋白,从而减轻与个体性别有关的恶化程度。
2、J Pineal Res:周舟组揭示褪黑素通过调控SERPINA3N依赖性神经炎症拮抗TMT引起神经毒性
三甲基氯化锡( Trimethyltin Chloride, TMT)是一种剧毒重金属化合物,能通过呼吸道、消化道及皮肤进入体内蓄积,半衰期长,造成毒性损伤。大量流行病学证据表明,TMT暴露是阿尔兹海默症等退行性神经疾病的高危因素之一,但是TMT神经毒性机制复杂,分子水平目前仍缺乏深入的研究。褪黑素(Melatonin)是由松果腺和其他器官合成,具有如调节昼夜节律,清除自由基和对抗炎症等多种生物学功能的生理性激素。Melatonin是否可以通过调节神经炎症来拮抗TMT诱导的脑损伤尚未见研究报道。
2019年7月30日,浙江大学公共卫生学院周舟教授、陆军军医大学皮会丰副教授课题组合作在Journal of Pineal Research(IF 15.221)在线发表研究论文。研究首次报道褪黑素通过调控SERPINA3N-依赖性神经炎症,从而有效逆转三甲基氯化锡引起的神经毒性。

研究首先建立TMT急性暴露引起中枢神经系统损伤的小鼠模型,并发现melatonin能有效逆转TMT急性暴露所造成的学习记忆损伤,并减少小鼠大脑海马区神经元丢失。随后应用TMT标记定量的蛋白组学技术与生物信息学分析发现SERPIAN3N是melatonin拮抗TMT引起神经毒性的关键分子靶点。
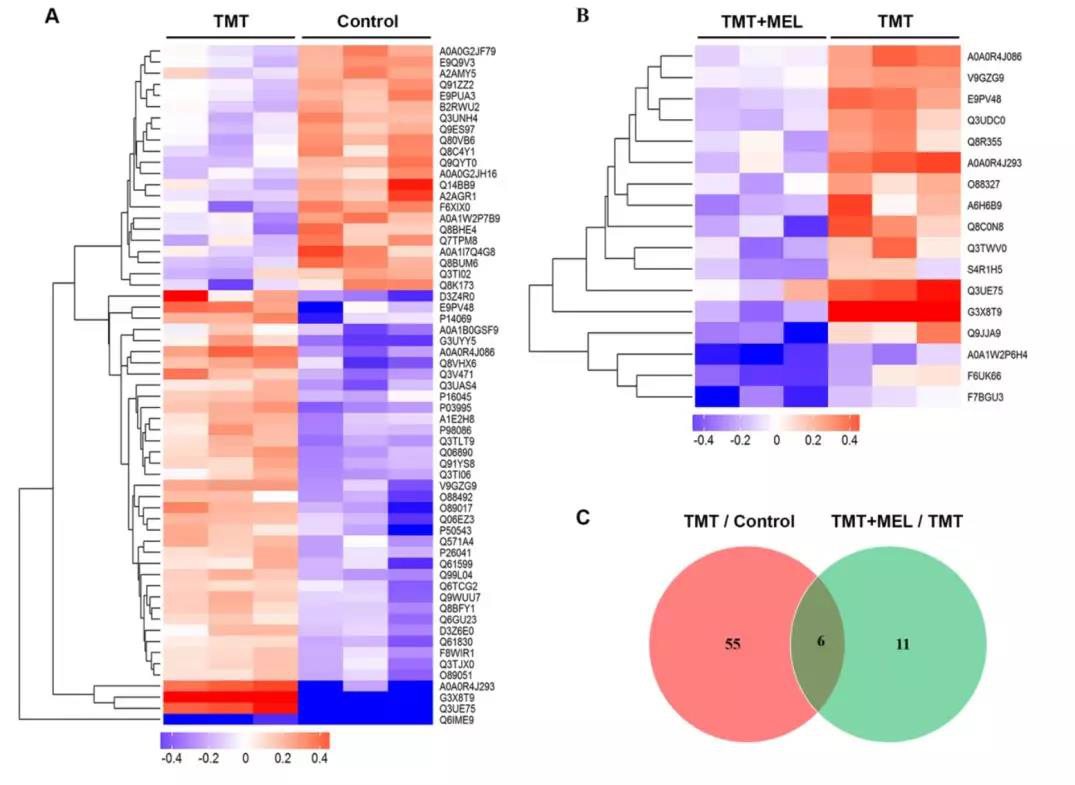
定量蛋白质组学分析小鼠海马区差异蛋白
进一步的机制研究发现,SERPINA3N特异性地表达于海马区星形胶质细胞,推测星形胶质细胞以及其相关神经炎症是TMT引起神经毒性的罪魁祸首。实验结果表明,melatonin可以有效减轻星形胶质细胞增殖和向A1型转化,同时减轻TMT引起的小鼠海马区炎性因子与炎性相关趋化因子的释放。当小鼠海马区过表达SERPINA3N蛋白后,有效阻断了melatonin对TMT引起神经毒性和神经炎症的保护作用,证明了抑制SERPINA3N依赖性神经炎症是melatonin拮抗TMT神经毒性的关键。该研究为发现melatonin的多种生物学功能,以及临床治疗重金属污染对公众健康造成的损害提供了新的视角。
参考文献
[1] Cristina Molnar, et al. (2019) The histone code reader PHD finger protein 7 controls sex-linked disparities in gene expression and malignancy in Drosophila, Science Advances. DOI: 10.1126/sciadv.aaw7965[2] Yu Xi, et al. (2019) Inhibition of SERPINA 3N‐dependent neuroinflammation is essential for melatonin to ameliorate trimethyltin chloride‐induced neurotoxicity. Journal of Pineal Research.
原创: Dr.Proteomics 精准医学与蛋白组学





 浙公网安备33010802007965号
浙公网安备33010802007965号